二、实验方法
1、二阶钯离子萃取
用盐酸把分析样品酸度调整至0.2N盐酸后,加入2毫升丁二酮肟溶液,5毫升0.1N EDTA溶液,搅匀并放置10分钟,用两份氯仿萃取之,每次1分钟,合并萃取液,并用0.2N盐酸洗涤后置于水浴上蒸干,残渣加几滴浓硫酸加热至透明。
2、钯的测定
取含钯不大于500微克的分析液一份加入5毫升1:1盐酸,10毫升20%的碘化钾溶液和2毫升l%抗坏血酸,在50毫升容量瓶中加水至刻度,以蒸馏水为空白液,在选定波长下测吸光度值。
三、实验结果与讨论
1、吸收曲线
在6个50毫升容量瓶中分别加入钯标准溶液0.1毫升,0.2毫升,0.3毫升,0.4毫升,0.5毫升和0.6毫升,浓度分别为0.1毫克/5O毫升,0.2毫克/5O毫升,0.3毫克/50毫升,0.4毫克/5O毫升,0.5毫克/50毫升,0.6毫克/5O毫升,按实验方法分别发色,测得不同波长时的吸光度如图1。
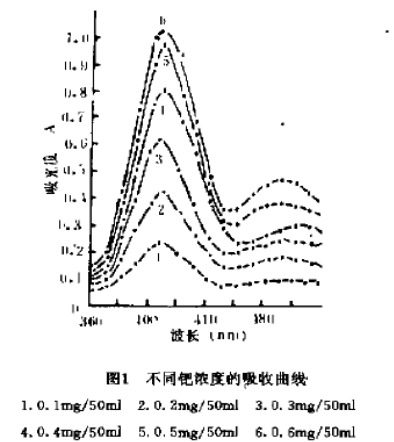
由图l看出,钯碘络合物的吸收曲线上有两个峰,分别在406纳米和490纳米处,选择406纳米波长作其它条件实验及样品测定,其灵敏度较高。
2、酸度的影响
取标准钯溶液5毫升(5毫克钯),稀释到50毫升则钯溶液浓度为0.1毫克/毫升,取8只50毫升容量瓶,分别加入上面配好的钯溶液l毫升,再分别加入不同体积的1:1盐酸溶液,按实验方法(上述)发色,同时测得pH值和吸光度,结果如图2。
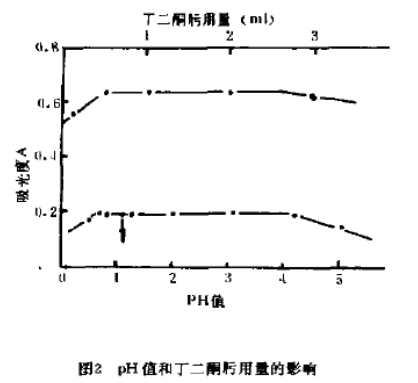
图2表明,pH值在0.7-3.5范围内钯碘络合物的吸光度最大且稳定不变。
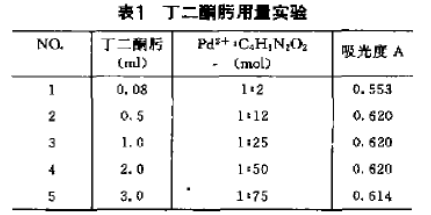
3、丁二酮肟用量实验
改变实验方法中的丁二酮肟用量。取0.1毫克/毫升标准钯溶液3.0毫升数份,在其它条件不变时测吸光度,结果如图2和表1。钯与丁二酮肟摩尔比为1:12-1:60时较为合适。
4、碘化钾用量实验
取0.1毫克/毫升标准溶液3毫升数份,按实验方法只改变碘化钾溶液量,其它条件不变,发色后测吸光度,如图3。
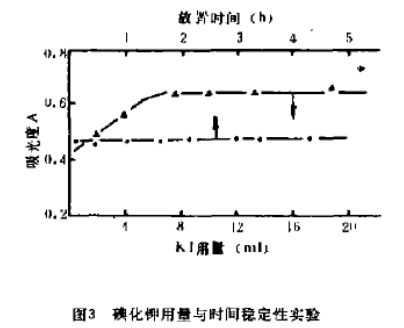
从图3中可看出当碘化钾用量大于7.5毫升时吸光度已达最大且不变。本实验选用10毫升碘化钾溶液较为合适。
5、钯碘络合物稳定性实验
取0.1毫克/毫升的钯标准溶液3毫升,按实验方法发色,每隔一定时间测吸光度,结果如图3。图3表明钯碘络合物生成迅速,反应完全,在酸性范围内测得4小时内吸光度是稳定的。
6、工作曲线
取8只50毫升容量瓶分别加入0.05-0.70毫克钯标准溶液,按实验方法发色测其吸光度,结果如图4。
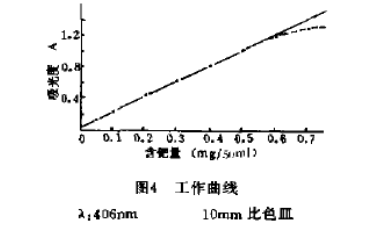
从图4中可看出工作曲线的线性范围。在50毫升溶液中,钯含量在0.05-0.50毫克范围内符合比尔定律。
 钯碳回收
钯碳回收
